以下、論文紹介と解説です。
Schlessinger J, et al. Safety, Effectiveness, and Pharmacokinetics of Crisaborole in Infants Aged 3 to < 24 Months with Mild-to-Moderate Atopic Dermatitis: A Phase IV Open-Label Study (CrisADe CARE 1). 2020; 21:275-84.
乳児は計137人(平均年齢 13.6±6.42か月)に関し、PDE4阻害薬クリサボロール軟膏の安全性と有効性を検討した。
背景
■ クリサボロール軟膏(2%)は、非ステロイド系のホスホジエステラーゼ4阻害剤であり、軽症から中等症のアトピー性皮膚炎(atopic dermatitis; AD)の治療薬である。
目的
■ 本研究の目的は、軽症から中等症のアトピー性皮膚炎のある生後3カ月から24カ月未満の乳児を対象とした非盲検試験において、クリサボロール軟膏の安全性、有効性、薬物動態(pharmacokinetics; PK)を評価することだった。
方法
■ Investigator's Static Global Assessment(ISGA)が軽症(2)または中等症(3)であり、治療可能な体表面積の割合(percentage of treatable body surface area; %BSA)が5以上の乳児(3~24カ月)に、クリサボロール軟膏を1日2回、28日間投与した。
■ また、ISGAが中等症で%BSAが35以上の集団をPK解析に含めた。
■ エンドポイントは、安全性(主要評価項目)、有効性、PK(探索的評価項目)だった。
結果
■ 対象となった乳児は計137人(平均年齢[SD] 13.6か月[6.42])で、PKを調べた集団は21人(12.7か月[6.58])だった。
■ 治療上の有害事象(Treatment-emergent adverse events; TEAE)は88人(64.2%)で報告された(98.9%が軽度/中等度と評価)。
■ TEAEは22人(16.1%)では治療に関連したものと考えられ、最も多く報告されたのは塗布部位の疼痛(3.6%)、塗布部位の不快感(2.9%)、紅斑(2.9%)だった。
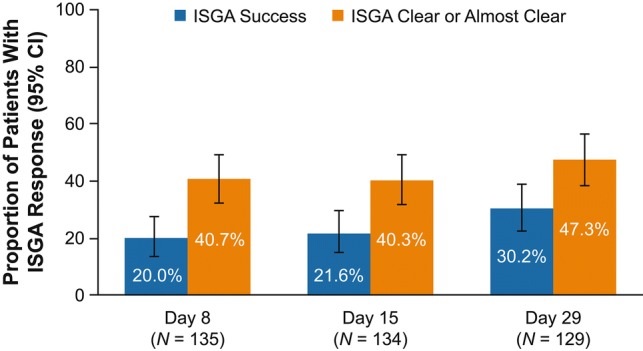
■ 29日目に2段階以上の改善を示したISGA(軽快/ほぼ軽快)を達成したのは30.2%だった。
論文より引用。ISGAの変化。
■ 試験開始から29日目までのEASI(Eczema Area and Severity Index)スコアの平均変化率は-57.5%、Patient-Oriented Eczema Measure(POEM)の総スコアの平均変化率は-8.5%だった。
論文より引用。EASIスコアの変化。
論文から引用。POEMの変化。
■ 非線形回帰分析に基づいた乳児におけるクリサボロールの全身曝露は、2歳以上の患者の曝露と同等だった。
結論
■ この非盲検試験では、軽症から中等症のADのある乳児(3~24ヵ月未満)において、クリサボロール軟膏は2歳以上の患者と同等の全身曝露で、良好な忍容性と有効性を示した。
スポンサーリンク(記事は下に続きます)
PDE4阻害薬は、2歳未満の乳児のアトピー性皮膚炎への適応が期待されています。

■ 2歳未満の顔のアトピー性皮膚炎は、多くの場合はステロイド外用薬で対応できるのですが、難渋する場合もあります。
■ その際に、ステロイド外用薬以外の抗炎症薬がつかえれば…と感じることもあります。
■ まだ当面は使用できる予定にはありませんが、この年齢の治療薬も、さらに発展してくる可能性がありますね。
■ PDE4阻害薬は、さらに十分な検討の上で日本でも使用できるようになってくれば…と思っています。
![]() 今日のまとめ!
今日のまとめ!
✅ PDE4阻害薬外用薬クリサボロール軟膏は、現在、生後3ヶ月からの検討が進んでいるようだ。